Zawodnicy uprawiający sport wyczynowo są szczególnie narażeni na urazy. Zawodnik jest cennym członkiem drużyny i niejednokrotnie zależy od niego wynik rywalizacji sportowej. Z tego powodu fizjoterapeuci sportowi robią wszystko aby przywrócić zawodnika do pełnej sprawności w możliwie najkrótszym czasie. Stąd też w procesie jego terapii zastosowana została m.in. laseroterapia wysokoenergetyczna.
Autorzy: Grzegorz Głąb, Rafał Obuchowicz, Krzysztof Klimek
Wprowadzenie
Urazy stawu skokowego są jednymi z częstszych uszkodzeń kończyny dolnej spotykanych w sporcie tak amatorskim jak i profesjonalnym. W zakresie samego stawu skokowego urazy powstające w skrajnej supinacji powodujące uszkodzenia więzadeł pobocznych stawu skokowego są najczęstsze. W sporcie zwłaszcza profesjonalnym bardzo istotna jest szybka regeneracja uszkodzeń i możliwie jak najwcześniejsze wprowadzenie kinezyterapii i treningu specjalistycznego, co daje możliwość szybkiego powrotu do aktywności sportowej. Coraz więcej prac badawczych potwierdza wpływ laseroterapii wysokoenergetycznej na przyspieszenie regeneracji tkanek miękkich. Wydaje się, że może ona znaleźć szerokie zastosowanie w leczeniu uszkodzeń narządu ruchu zwłaszcza w sporcie wyczynowym.
Cel badania
Celem badania była ocena efektów laseroterapii wysokoenergetycznej u piłkarza ręcznego po uszkodzeniu więzadeł stawu skokowego.
Opis badania
Badanie przeprowadzono u piłkarza ręcznego z uszkodzeniem III stopnia (zerwanie) więzadła skokowo-strzałkowego przedniego (ATFL) i II stopnia (naderwanie znacznego stopnia) więzadła piętowo-strzałkowego (CFL) ocenionego na podstawia badania USG.
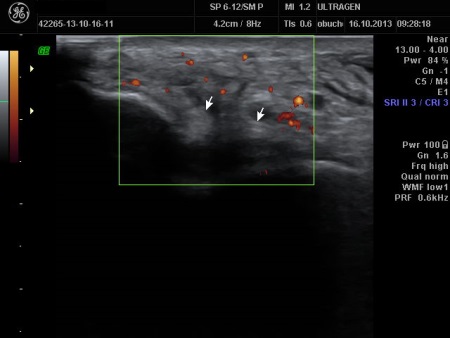
Obraz ultrasonograficzny więzadła skokowo-strzałkowego przedniego – stan po 24 godzinach od urazu
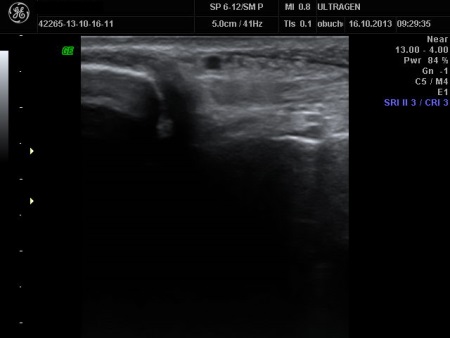
Obraz ultrasonograficzny więzadła piętowo-strzałkowego – stan po 24 godzinach od urazu
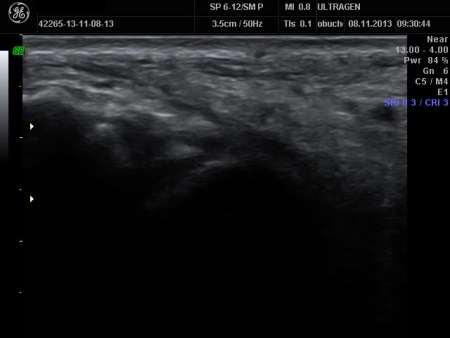
Badanie kontrolne po 25 dniach od urazu ATFL – obraz uformowanej blizny bez cech przekrwienia
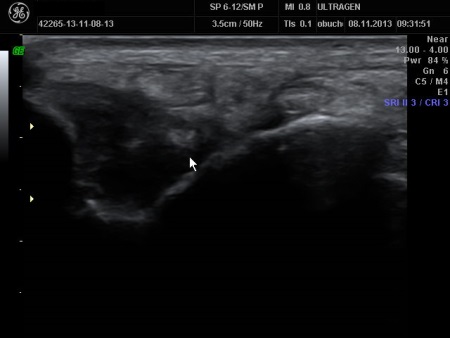
Badanie kontrolne 25 dni po urazie – obraz wygojonego CFL bez cech zmian obrzękowych
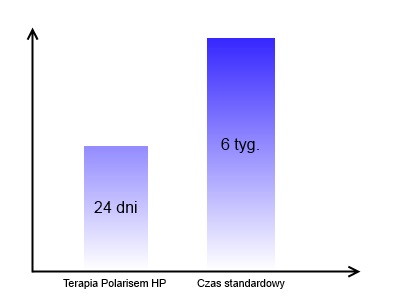
Bezpośrednio po urazie zastosowano chłodzenie, ucisk i uniesienie chorej kończyny. Od drugiego dnia po urazie stosowano laseroterapię wysokoenergetyczną. Wykonano 12 zabiegów z częstotliwością co 2 dni, ponadto stosowano głęboki masaż poprzeczny, a po tygodniu wprowadzono trening stabilizacji centralnej oraz trening propriocepcji. Zabiegi laseroterapii wysokoenergetycznej wykonywano przy użyciu urządzenia Polaris HP firmy Astar o długości fali 808 nm i 980 nm o mocy od 1 do 5 W dla każdego ze źródeł w dawce od 10 do 30 J/cm2, wypełnienie od 20 do 80% ze stopniowaniem zarówno mocy jak i dawki oraz współczynnika wypełnienia. W pierwszych 4 zabiegach stosowano częstotliwość 3000 Hz a następnie 700 Hz. Zabieg wykonywano metodą dynamiczną w obszarze obrzęku i uszkodzonych więzadeł. W literaturze ortopedycznej przyjmuje się okres 6 tygodni za podstawowy czas gojenia pozwalający na inicjację procesu, oraz wytworzenie zrostu szczególnie w przypadku uszkodzeń całkowitych obejmujących przerwanie ciągłości więzadła z wytworzeniem kikutów okres od uszkodzenia do pełnej integracji włókien może nawet przekraczać 6 tygodni. W prezentowanym przypadku okres powyższy uległ znacznemu skróceniu. Pierwsze badanie wykazało uszkodzenie III stopnia ATFL ale już kolejne wykonane po 2 tygodniach pokazało integrację kikutów w postać wydolnej blizny, jej modelowanie, a resorpcja wysięku oraz zmian obrzękowych odbyła się w ciągu kolejnych 9 dni. Proces ten był uogólniony – dotyczył całego obszaru objętego terapią – w zakresie uszkodzonego CFL obserwowano podobny proces. Więzadło uszkodzone częściowo (stopień II) uległo znacznego stopnia wygojeniu i redukcji zmian obrzękowych już po 14 dniach. Zawodnik po pięciu tygodniach od wystąpienia urazu powrócił do pełnej aktywności sportowej, nie występował obrzęk stawu, a badany nie zgłaszał żadnych dolegliwości bólowych.
Wnioski
Zastosowanie laseroterapii wysokoenergetycznej istotnie skróciło okres regeneracji, co umożliwiło znacznie szybszy powrót do aktywności sportowej zawodnikowi po uszkodzeniu więzadeł stawu skokowego.